La co-infection VIH/tuberculose à pleins tubes
1,2 million d’individus dans le monde sont co-infectés par Mycobacterium tuberculosis, la bactérie responsable de la tuberculose, et le virus du Sida (VIH-1). Cette association est meurtrière : elle complique le diagnostic et le traitement des patients, et augmente la pathogénicité de ces deux agents infectieux. Une collaboration internationale, menée par des chercheurs du CNRS et de l’Inserm, a mis en évidence que dans un contexte tuberculeux, le VIH-1 passe d’une cellule à l’autre grâce à des nanotubes formés entre les macrophages, ce qui augmente très fortement la proportion de cellules infectées. Ces résultats sont publiés le 26 mars 2019 dans la revue Cell Reports.
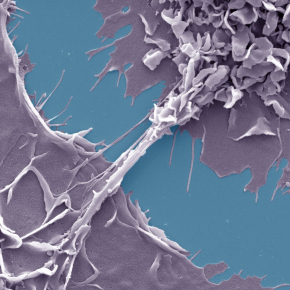
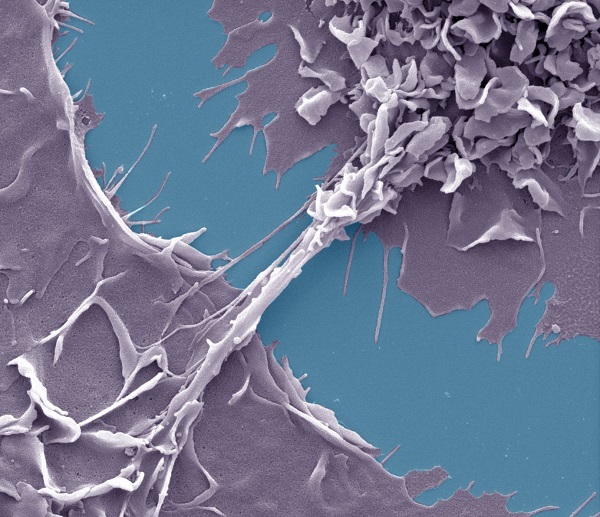
Des chercheurs de l’Institut de pharmacologie et de biologie structurale (CNRS/Université Toulouse III – Paul Sabatier) et du Laboratoire international associé IM-TB/VIH établi entre le CNRS et le Conicet (Argentine), en collaboration avec le Centre de physiopathologie de Toulouse Purpan (CNRS/Inserm/Université Toulouse III – Paul Sabatier), ont montré que les macrophages, cellules hôtes pour la tuberculose et pour le VIH-1, forment entre eux des nanotubes lorsqu’ils sont exposés à l’interleukine-10 (IL-10), une molécule sécrétée en cas de tuberculose. L’abondance dans les poumons de ces macrophages particuliers, appelés M(IL-10), est corrélée avec la gravité de la maladie. Les nanotubes sont empruntés par les particules virales du Sida, comme des tunnels, pour infecter les cellules voisines et s’y multiplier. En inhibant leur formation par différentes approches, les scientifiques ont réussi à réduire le transfert du virus entre les macrophages, entrainant ainsi une diminution de la production de VIH-1.
En cas de tuberculose sévère, la formation de nanotubes entre les macrophages est amplifiée, facilitant par conséquent la dissémination du virus du Sida et augmentant ainsi la production virale. La présence de ces macrophages particuliers pouvant être quantifiée, le diagnostic et le suivi de la tuberculose chez les patients co-infectés pourra être facilité. Ces travaux ouvrent ainsi la voie à de nouvelles approches thérapeutiques visant à contrôler l’augmentation de la charge virale en cas de tuberculose.
Tuberculosis exacerbates HIV-1 infection through IL-10/STAT3-dependent tunneling nanotube formation in macrophages. Souriant S, Balboa L, Dupont M, Pingris K, Kviatcovsky D, Cougoule C, Lastrucci C, Bah A, Gasser R, Poincloux R, Raynaud-Messina B, Al Saati T, Inwentarz S, Poggi S, Moraña EJ, Gonzalez-Montaner P, Corti M, Lagane B, Vergne I, Allers C, Kaushal D, Kuroda MJ, Sasiain MDC, Neyrolles O, Maridonneau-Parini I, Lugo-Villarino G, Vérollet C. Cell Reports, le 26 mars 2019. DOI : 10.1016/j.celrep.2019.02.091. https://www.cell.com/cell-reports/fulltext/S2211-1247(19)30277-3